黑碳是陆地生物质与化石燃料的不完全燃烧生成富碳的残留物,广泛的炭化温度促使生物聚合物转变为高度浓缩多环芳香族化合物,进而形成黑碳连续体。我国每年约产生14亿t农业废弃生物质,潜在生成约4.2亿t黑碳[1]。黑碳广泛存在于大气、土壤、水体和沉积物等环境介质中,参与了重要的地质和环境效应过程,如土壤理化性质调节、土壤碳封存和污染物吸附等[2-4]。黑碳的分子结构高度芳香化,具有一定的生物化学稳定性。黑碳的存在增强了土壤碳储存的潜力,对土壤有机碳库的稳定具有极其重要的作用,从而对生态系统的碳循环产生长期的潜在影响。前人通过量化土壤碳库总量发现其远大于黑碳历史累积量,表明黑碳存在潜在的支出项——溶解态黑碳(dissolve black carbon, DBC) [5]。
DBC是黑碳连续体的可溶性部分,普遍存在于河流、海洋和土壤等环境介质中,是连接陆地土壤与河流底泥黑碳库之间的重要纽带,在全球碳循环过程中起着关键作用。前人在河流溶解有机质(dissolved organic matter, DOM)中检测到贫氢分子(H/C比例<1)和高度不饱和多环芳烃结构,其来源被认为是陆源BC的径流输入[6]。Hockaday等[7]在土壤水溶性有机质中发现稠芳香环结构分子的存在,表明土壤BC可以降解并以溶解态的形式进入DOM库。DBC含有的稠环芳香结构和含氧官能团,可同一些疏水性有机物和重金属发生吸附/络合作用。DBC是重要的天然光敏剂,在可见光和紫外光波段范围内均有吸收,在光照激发后可以通过间接光反应产生多种活性中间体(reactive intermediate, RIs),如单线态氧(1O2)、羟基自由基(·OH)、超氧阴离子(O2·-)及激发三线态(3DBC*)等,对水生环境中有机污染物和微量金属的环境归趋产生重要的影响。
DBC是溶解有机碳(dissolved organic carbon, DOC)的重要组成部分,约占河流DOC的10%,海洋中DOC的2%[5, 8],这种耦合表明DBC释放到水生生态系统的生物地球化学机制与DOC相似。Yamashita等[9]证实不同流域中DBC与DOC从土壤到河流的迁移机制相似,且水体中DBC与DOC两者浓度呈线性相关。Xu等[10]对长江、黄河和东海沿岸DBC、颗粒BC进行测量,长江水体DBC/DOC值为(3.0±0.4)%,黄河水体DBC/DOC值为(4.8±3.6)%,东海沿岸DBC/DOC值为(3.4±0.6)%。即使不同流域中DBC/DOC值有所不同,从流域尺度扩大到全球尺度,也观察到两者浓度之间的正相关性(CDBC=0.054×CDOC-0.022,P<0.01) [9, 11],通过这种线性关系可对DBC的全球碳通量进行估算。
有关DBC的研究起步于2004年,主要集中在定性识别、定量检测及其空间分布等方面。而关于DBC的环境行为及其对污染物迁移转化的影响效应,尚缺乏统一的认识和理解。本文基于现有研究DBC的相关文献进行了回顾和梳理,总结了DBC的来源与赋存、特征分析、结构与特征和环境效应。归纳了DBC对有机污染物和重金属等迁移转化影响等方面的研究进展,重点评述了DBC在碳循环中的作用、DBC污染物的吸附作用、DBC对污染物氧化还原作用和光化学转化影响等相关研究,并在此基础上探讨了现有研究中存在的相关问题,展望了未来研究方向的发展。
1 溶解态黑碳的来源与赋存(Source and occurrence of dissolved black carbon)
黑碳是疏水性颗粒物,不溶于水。DBC是一类通过高温缩聚形成的稠环芳香化合物,分子结构中含有亲水性官能团,可溶于水。前人对天然水体中DOC结构分析发现,DOC中存在黑碳可溶性的部分,这类性质不同于黑碳,但稠芳香环结构、表面活性官能团等组分又与黑碳相似的物质引起了人们的广泛关注[6-7, 12]。Masiello和Druffel[12]提出河流中DOM中存在可溶性碳这一概念,揭开了DBC研究的序幕。Kim等[6]利用电喷雾电离与超高分辨率质谱等技术,分析鉴定DOM样品,证实了DOM中存在可溶性碳部分。Jaffé等[5]对土壤木炭产物进行量化研究发现,木炭产物总量通过溶解和迁移至河流海洋而降低,除了被完全氧化成CO2和颗粒侵蚀外,木炭产物还以溶解的形式释放到水体环境。
DBC来源分为自然来源和人为来源[13]。自然来源包括火山喷发的产物、森林火灾产生的黑碳和动物粪便等材料中可溶于水的部分,具有区域性和偶然性;人为来源包括生物炭的运用、生物质燃烧、汽车尾气排放、垃圾焚烧和工业排放废渣等材料中可溶于水的部分,具有长期性和持续性。DBC可来源于陆地土壤中黑碳的降解。新生成的黑碳能降解出少量的DBC,山火事件的发生短期内对流域内DBC的浓度影响非常小[14],但陈年黑碳在老化和降解过程中会产生更多的DBC。DBC受到地表径流和冲刷渗透等作用从地层中迁移,进入河流、湖泊等水体,再由河流迁移至海洋。通过地层迁移的DBC是海洋DOM池中有机碳的重要来源。水溶性有机碳的来源测定分析表明,除了河流等水体输入,粉尘与生物质燃烧后烟尘的大气沉积过程也是海洋DBC重要来源[15]。Khan等[16]通过对南极湖泊表层水体中DBC缩聚程度变化的研究,表明该水体中DBC的主要来源是化石燃料和生物质不完全燃烧后的烟尘沉降。
DBC在受火灾影响的河口、近海沿岸含量丰富,但在多年未受火灾影响的流域和极地地区的冰川河流中仍有检出,其来源是烟尘的大气沉降过程。DBC约占全球河流通量溶解有机碳的10%[5],包括近海沿岸DOM的4%~7%和海洋DOM的4%~22%。河流中DBC在受人为干扰频繁区域通常稠环缩聚程度较低,人为活动较少区域缩聚程度高。Dittmar等[8]对Paraíba do Sul河的DBC负荷开展了研究,结果表明人类活动对流域中DBC的含量和芳香结构有影响,并确定了DBC在分子水平上为多环芳香碳的总和。Fang等[17]发现在渤海、东海沉积物中,DBC沉积通量与近150年来我国社会经济发展具有阶段性耦合关系。
河流汇入过程是DBC在全球碳循环中的一个主要陆地-海洋通量。海洋是DBC的最终储存库,刚果河每年向海洋输出约8.03×105 t的DBC,大约比颗粒黑碳多50%[18]。DBC广泛存在于各类水体环境中,浓度具有明显的时空差异。河流和海洋水体中DBC的浓度均具有显著的时空三维变化特征[19]。DBC在水平空间上呈现河流-近岸-近海-远海明显递减的趋势;但在垂直空间上浓度变化很小。
一是由于DBC结构相对稳定,短时间内不会发生物理、化学等反应;二是潮汐等水动力作用将水体上下混合均匀。DBC的聚集行为是影响垂向水体质量通量的重要因素。土壤释放到水体的DBC在垂直方向上可能发生聚集行为,沉降在河流或河口沉积物中,影响河流输出强度[20]。河流与海洋中的DBC浓度具有很强的季节性特点。渤海地区由于冬季具有强劲的风生流使水动力作用增强,因此含有较高浓度DBC的近岸水体向外扩散,使水体中DBC浓度明显高于其他季节。DBC在土壤-地下水中可能的来源与环境行为如图1所示。
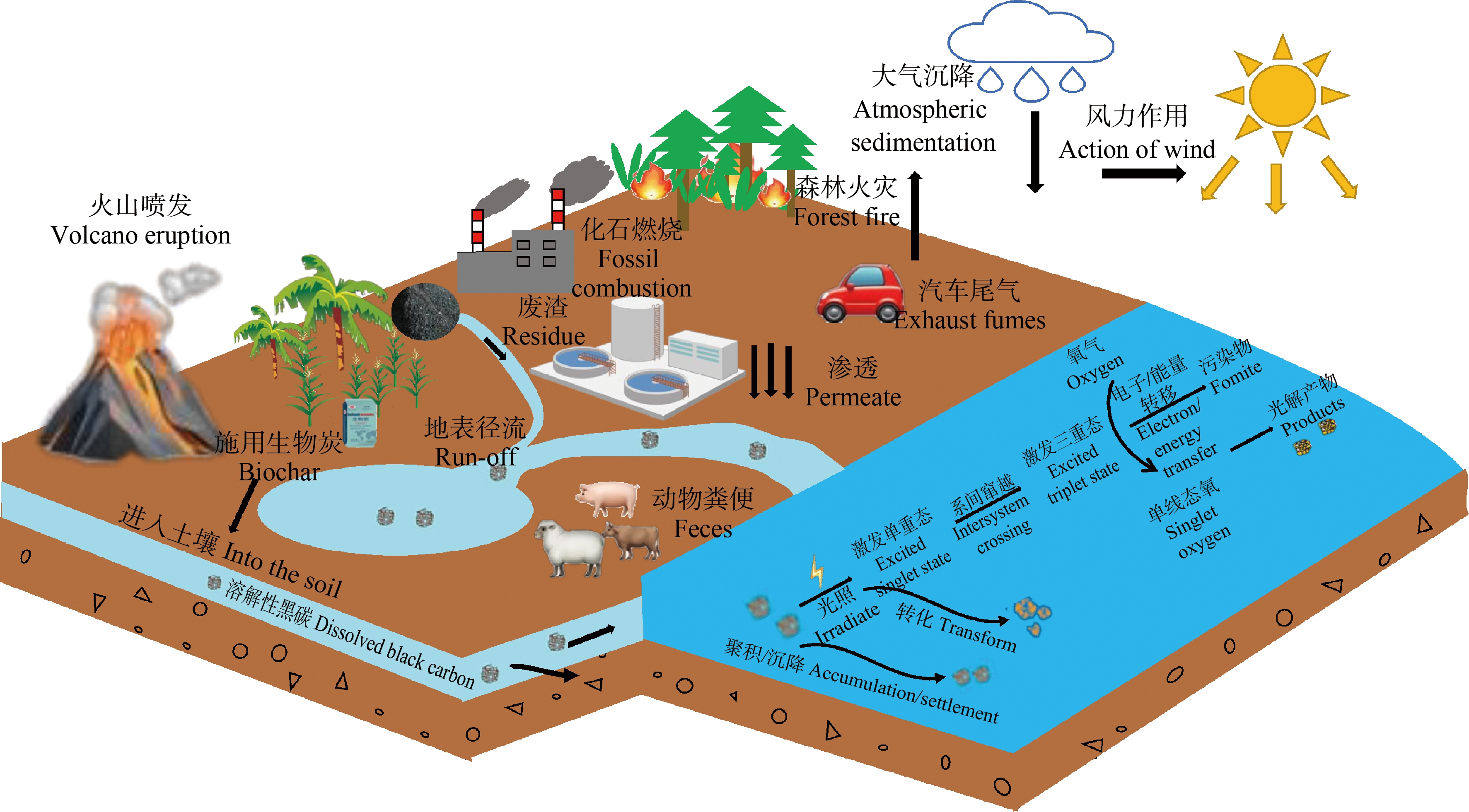
图1 溶解态黑碳来源与环境行为
Fig. 1 Sources and environmental behaviors of dissolved black carbon
2 溶解态黑碳的特征分析(Characteristic analysis of dissolved black carbon)
DBC结构多样、成分复杂、物理化学性质独特。自发现以来,DBC的来源、结构表征、特性描述及其与DOM的差别一直是国内外研究的热点。DBC分析的方法由定性识别逐渐深入到定量研究。目前苯多羧酸法是DBC识别和定量的较可靠的方法之一,结合液相/气相色谱-质谱分析此方法中DBC的消解产物[21]。苯多羧酸法是分析DBC稠环芳香簇结构的分子标志物法,根据测量的苯多羧酸(BPCA)浓度估算DBC浓度。BPCA法产生的氧化产物由苯环组成,苯环带有3个(B3CA)、4个(B4CA)、5个(B5CA)和6个(B6CA)羧基,这些羧基是缩聚芳香结构化学降解后形成的。B6CA与总测量BPCA的相对比例越大,表示缩聚芳香结构越多,而B3CA和B4CA的相对比例越大,则缩聚芳香结构越少。BPCA法的原理是在高温高压环境下利用浓硝酸将DBC的稠环结构氧化成一系列BPCA,继而定量检测BPCA,并利用BPCA-DBC转化公式得到DBC的含量。Stubbins等[22]提出DBC浓度可通过BPCA浓度进行换算:
CDBC = 12.01×0.0891×(C B6CA + C B5CA)0.9175
公式在DBC完全被消解、全部转化为BPCA条件下使用,是一种理想公式。但在实际中存在消解流程不同、DBC分子消解不完全等情况,使得该公式计算出的DBC含量为保守值,结果缺少可比性。现阶段尚未有成熟完整的技术对DBC进行表征,在传统的表征手段(如元素分析、紫外-可见光谱(UV-Vis)、核磁共振波谱、傅里叶红外光谱(FT-IR)等)获取的信息基础上,定量13C固体核磁(13C DP/MAS NMR)和辐射技术的发展和应用,为解析DBC的结构、探索DBC对污染物质影响作用机制创立了优越条件。Liu等[23]通过NMR对生物炭衍生的DBC分析,阐明DBC具有丰富的脂肪族碳与羧基碳。Qu等[24]根据FT-IR和NMR对DBC表征结果发现,DBC主要由羧基和少量脂肪族碳的芳香簇组成。这些结果表明,对于不同生物质衍生的DBC元素组成和比例还缺乏规律性共识,需要进一步研究。在表1中简要归纳了现阶段的一些表征技术。
表1 溶解态黑碳(DBC)的表征
Table 1 Characterizations of dissolved black carbon (DBC)

表征技术Characterization technique目的Intention结果Result参考文献Reference13C核磁共振技术(13C NMR)13C NMR technology表明DBC平均脂肪碳和O/N取代脂肪碳比值It indicates that the mean fat carbon of DBC and the ratio of O/N substituted fat carbonDBC中有较多的羧基碳、较高的芳香碳和较少的脂肪族碳DBC has more carboxyl carbon, higher aromatic carbon, and less aliphatic carbon[20, 24-25]紫外-可见光谱分析(UV-vis)Ultraviolet-visible (UV-vis)描述DBC的相对分子量和芳香性等特征Describe the relative molecular weight and ar-omaticity of DBCDBC中芳香类物质含量高,存在共轭体系和生色团DBC has high aromatic content, and existence of conju-gated system and chromophore[26-28]三维荧光光谱(EEM)Fluorescence excitation-emission matrix (EEM)提取不同荧光组分信息,对DBC进行定性和半定量研究Extract information of different fluorescent components, and conduct qualitative and semi-quantitative research on DBCDBC含有低分子量类腐殖酸化合物,高温会促进类腐殖酸物质的分解,产生更小、更简单的DBC结构DBC contains humic acid compounds with low molecu-lar weight; and high temperature will promote the de-composition of humic acid like substances, resulting in smaller and simpler DBC structures[29-30]X射线光电子能谱(XPS)X-ray photoelectron spectroscopy (XPS)半定量分析DBC官能团结构,表征DBC元素组成与极性指数Semi quantitative analysis of DBC functional group structure, characterization of DBC ele-ment composition and polarity indexDBC含有羧基、羟基、烷氧基等极性官能团,随着热解温度的升高,DBC中醌基团的含量增加、C—O基团含量降低、吡啶N和吡咯N含量降低DBC contains carboxyl, hydroxyl, alkoxy and other po-lar functional groups; with the increase of pyrolysis temperature, the content of quinone group in DBC in-creases, the content of C—O group decreases, and the content of pyridine N and pyrrole N decreases[31-33]傅里叶红外光谱(FT-IR)Fourier transform infrared (FT-IR)鉴定DBC组成和结构Identify DBC composition and structureDBC含有大量的—OH和C—O/C—O—C基团和苯环DBC contains a large number of —OH and C—O/C—O—C groups and benzene rings[34]
3 溶解态黑碳结构与性质(Structure and properties of dissolved black carbon)
DBC是BC中活跃的组分,由于其水溶性较强,易在环境介质中发生迁移。DBC分子带负电,其Zeta电位一般随着热解温度升高而增加[35]。DBC的形态不规则,粒径不均匀,平均粒径约为5.32 nm[36],被认为是一种碳量子点(粒径<10 nm的碳纳米颗粒)。DBC的平均分子质量较低,低分子量的DBC含有更多羰基结构。DBC元素组成具有富碳贫氢的特点,主要元素为C、O,含有少量H和微量N、S等[20, 37]。O/C值与分子中含氧官能团含量正相关,H/C值与分子的脂肪化和芳香程度负相关。水稻BC和DBC的O/C比分别为0.63和0.69;H/C比分别为0.04和0.08,说明DBC比BC含有更多的含氧官能团如羰基、羧基等,脂肪链结构含量更高[29]。DBC是一类稠环芳香族化合物,分子结构具有以下特征:5~8个苯环浓缩形成一个稠环芳香核(大部分情况为7个苯环)[38],芳香核的外围含有羧基、羟基、亚硝基、脂肪烃等取代官能团,并以羧基和羟基为主,酚基含量较少。
DBC具有疏水微区、芳香微域结构和微孔等结构,是菲、氯化苯等有机污染物和Cd(Ⅱ)、Pb(Ⅱ)等重金属离子的重要载体,并借由这些结构改变非极性污染物的水溶性。此外,生物质衍生的DBC含有腐殖质类成分、多环芳烃、木质素、微生物分解产物、蛋白质类成分等不饱和结构,可改良土壤性质、影响土壤微生物群落。在表2中对溶解态黑碳结构与理化性质之间的关系进行了简要的梳理总结。
表2 溶解态黑碳结构与性质的关系
Table 2 Relationship between structure and properties of dissolved black carbon
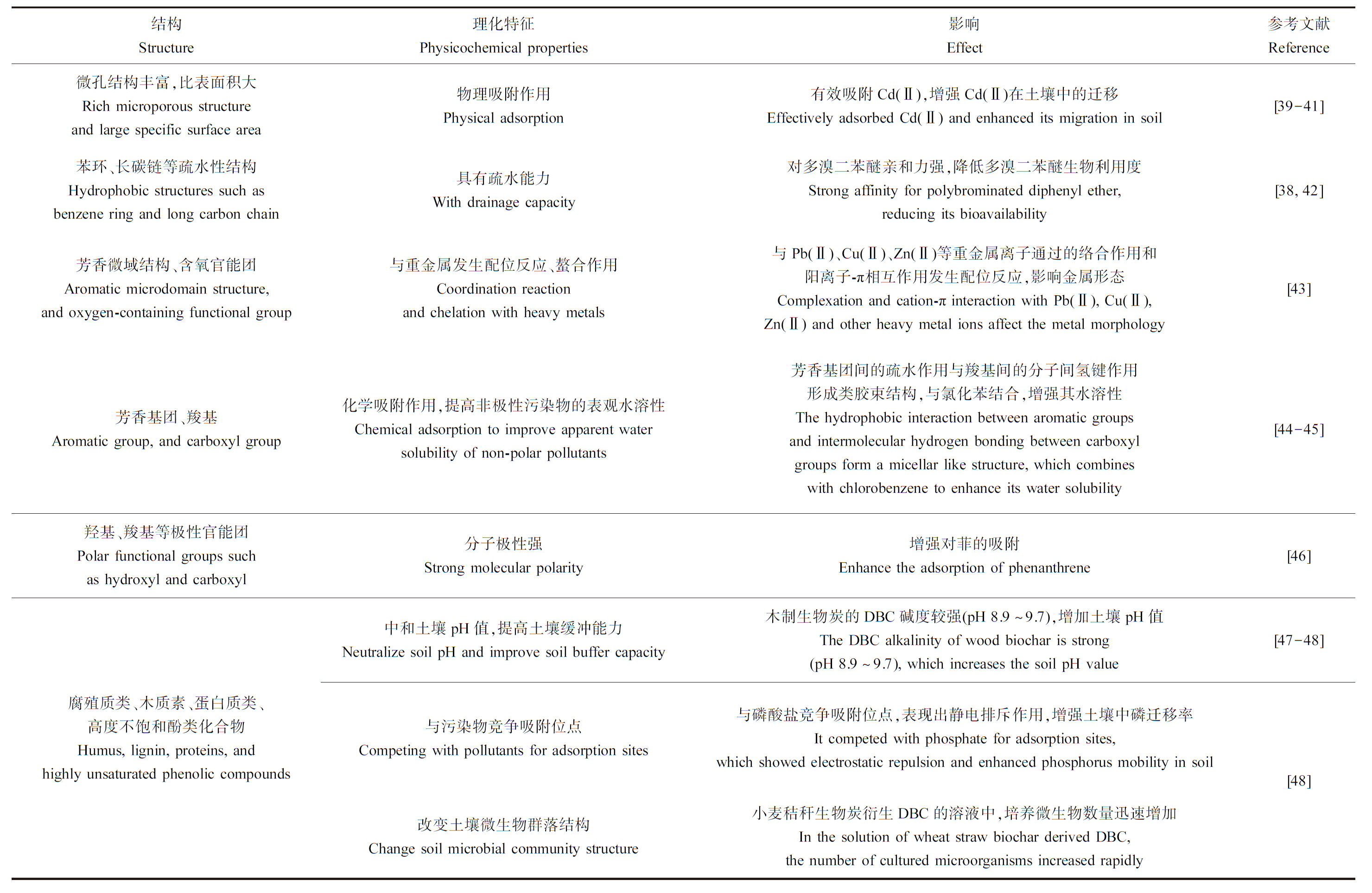
结构Structure理化特征Physicochemical properties影响Effect参考文献Reference微孔结构丰富,比表面积大Rich microporous structureand large specific surface area物理吸附作用Physical adsorption有效吸附Cd(Ⅱ),增强Cd(Ⅱ)在土壤中的迁移Effectively adsorbed Cd(Ⅱ) and enhanced its migration in soil[39-41]苯环、长碳链等疏水性结构Hydrophobic structures such asbenzene ring and long carbon chain具有疏水能力With drainage capacity对多溴二苯醚亲和力强,降低多溴二苯醚生物利用度Strong affinity for polybrominated diphenyl ether,reducing its bioavailability[38, 42]芳香微域结构、含氧官能团Aromatic microdomain structure,and oxygen-containing functional group与重金属发生配位反应、螯合作用Coordination reactionand chelation with heavy metals与Pb(Ⅱ)、Cu(Ⅱ)、Zn(Ⅱ)等重金属离子通过的络合作用和阳离子-π相互作用发生配位反应,影响金属形态Complexation and cation-πinteraction with Pb(Ⅱ), Cu(Ⅱ), Zn(Ⅱ) and other heavy metal ions affect the metal morphology[43]芳香基团、羧基Aromatic group, and carboxyl group化学吸附作用,提高非极性污染物的表观水溶性Chemical adsorption to improve apparent water solubility of non-polar pollutants芳香基团间的疏水作用与羧基间的分子间氢键作用形成类胶束结构,与氯化苯结合,增强其水溶性The hydrophobic interaction between aromatic groups and intermolecular hydrogen bonding between carboxylgroups form a micellar like structure, which combineswith chlorobenzene to enhance its water solubility[44-45]羟基、羧基等极性官能团Polar functional groups suchas hydroxyl and carboxyl分子极性强Strong molecular polarity增强对菲的吸附Enhance the adsorption of phenanthrene[46]腐殖质类、木质素、蛋白质类、高度不饱和酚类化合物Humus, lignin, proteins, andhighly unsaturated phenolic compounds中和土壤pH值,提高土壤缓冲能力Neutralize soil pH and improve soil buffer capacity木制生物炭的DBC碱度较强(pH 8.9~9.7),增加土壤pH值The DBC alkalinity of wood biochar is strong(pH 8.9~9.7), which increases the soil pH value与污染物竞争吸附位点Competing with pollutants for adsorption sites与磷酸盐竞争吸附位点,表现出静电排斥作用,增强土壤中磷迁移率It competed with phosphate for adsorption sites, which showed electrostatic repulsion and enhanced phosphorus mobility in soil改变土壤微生物群落结构Change soil microbial community structure小麦秸秆生物炭衍生DBC的溶液中,培养微生物数量迅速增加In the solution of wheat straw biochar derived DBC, the number of cultured microorganisms increased rapidly[47-48][48]
DOM对离子吸附能力的强弱,与自身结构(包括含氧官能团量、分子量、分子尺寸等)和电化学性质相关。与土壤和水体中含量丰富的富里酸(fulvic acid, FA)相比,DBC对离子的吸附能力可能会强于FA。DBC和FA对金属阳离子都具有很强的吸附能力,两者具有的含氧官能团和负电荷,可分别通过化学络合和静电吸引增加金属阳离子的表观吸附。DBC的H/C值在0.051~0.069之间,低于FA(H/C值为0.068~0.083)[49],表明DBC具有更高的芳香性,对阳离子的化学吸附作用更强。研究表明,DBC中的羧基、酚基等含氧官能团量和极性官能团高于FA[49-50],暗示对阳离子具有更强的络合作用。此外,DBC分子量和分子尺寸均低于FA,可能具有更大的比表面积和表面微孔结构,对离子具有更大的吸附容量。同时,DBC含有的矿物质也增强了对离子的吸附作用[41]。DBC具有带负电荷的位点,吸附各种阳离子,包括竞争性阳离子吸附和阳离子交换反应。而FA属于弱聚合物酸,只在特定pH(3~10)条件下才具有带负电荷的位点。当阳离子充当连接带负电荷的表面位点和极性基团的桥梁时,就会形成阳离子桥。FA借由阳离子桥机制,以表面配合物的形式与阴离子结合[51]。目前关于DBC对阴离子吸附的研究还未有报道。但DBC对阳离子的吸附能力强于FA,且极性官能团量较多,预计形成的阳离子桥种类和数量更加丰富,对阴离子的结合能力更强。
DBC含有芳香结构中的共轭体系、羧基和羰基等发色团,能够吸收紫外-可见光,发生光降解。光降解是DBC在表层水体中的主要转化途径,结构从高稠环浓缩形态转变为较低的稠环浓缩程度形态,在环境中的稳定性增强。光降解优先针对DBC结构中的芳香族和甲基部分,生成CH2/CH/C和羧基/酯/醌官能团,导致DBC芳香性降低。DBC水溶液经模拟光照28 d后,95%的DBC被降解[52],证实光降解是DBC的主要降解途径。高稠环浓缩程度DBC比低稠环浓缩程度的DBC更易发生光降解,未降解或部分降解的DBC随大洋热盐环流循环进行迁移,最终沉积水体深处。Qu等[24]比较DBC在氙灯照射前后的结构变化,发现光照7 d后DBC的吸光度明显下降。Fu等[33]通过紫外分光光度计和荧光光谱仪发现竹子衍生的DBC在氙灯照射169 h后254 nm处的吸收损失了56%。
DOM的光化学活性决定其地表水中污染物环境归趋的重要过程。DOM在光照下生成RIs,其量子产率与分子量大小和羰基、芳香酮等官能团的含量有关。3DOM*与1O2的量子产率与羰基含量正相关,3DOM*作为产生O2·-的前体物质,其羰基含量也影响O2·-的量子产率[53]。在表3中简单分类归纳了DOM的结构和光化学性质,旨在突出DBC较其他类DOM具有更强的光化学活性。
表3 溶解态黑碳和溶解性有机质的光活性及其对有机污染物光化学转化的影响
Table 3 Photo-activity of dissolved black carbon and dissolved organic matter, mediated phototransformation of organic pollutants
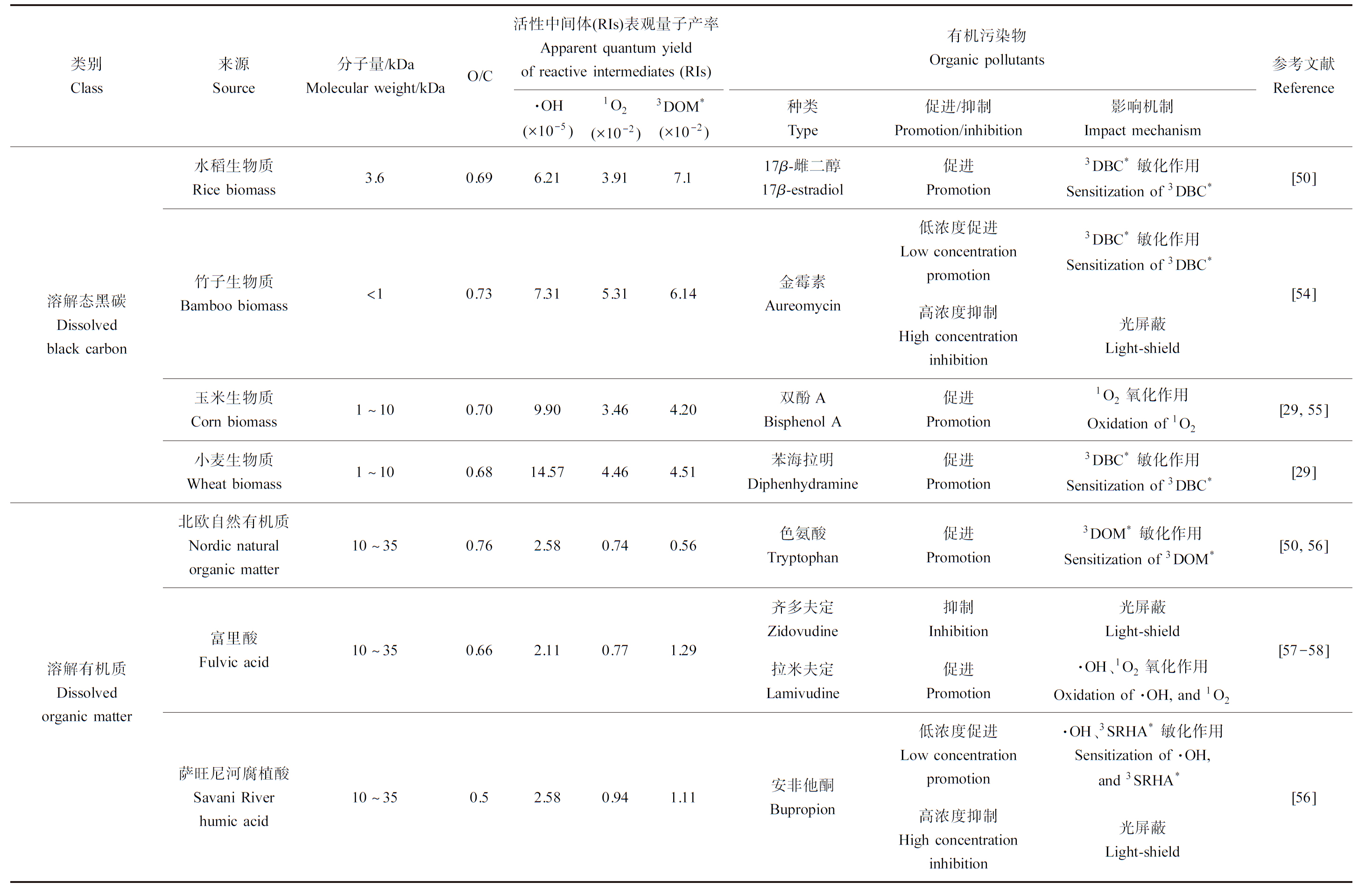
类别Class来源Source分子量/kDaMolecular weight/kDaO/C活性中间体(RIs)表观量子产率Apparent quantum yield of reactive intermediates (RIs)有机污染物Organic pollutants·OH(×10-5)1O2(×10-2)3DOM*(×10-2)种类Type促进/抑制Promotion/inhibition影响机制Impact mechanism参考文献Reference溶解态黑碳Dissolved black carbon水稻生物质Rice biomass3.60.696.213.917.117β-雌二醇17β-estradiol竹子生物质Bamboo biomass<10.737.315.316.14金霉素Aureomycin玉米生物质Corn biomass1~100.709.903.464.20双酚ABisphenol A小麦生物质Wheat biomass1~100.6814.574.464.51苯海拉明Diphenhydramine促进Promotion3DBC*敏化作用Sensitization of 3DBC*低浓度促进Low concentration promotion3DBC*敏化作用Sensitization of 3DBC*高浓度抑制High concentration inhibition光屏蔽Light-shield促进Promotion1O2氧化作用Oxidation of 1O2促进Promotion3DBC*敏化作用Sensitization of 3DBC*[50][54][29, 55][29]溶解有机质Dissolved organic matter北欧自然有机质Nordic natural organic matter10~350.762.580.740.56富里酸Fulvic acid10~350.662.110.771.29萨旺尼河腐植酸Savani River humic acid10~350.52.580.941.11色氨酸Tryptophan齐多夫定Zidovudine拉米夫定Lamivudine安非他酮Bupropion促进Promotion3DOM*敏化作用Sensitization of 3DOM*抑制Inhibition光屏蔽Light-shield促进Promotion·OH、1O2氧化作用Oxidation of ·OH, and 1O2低浓度促进Low concentration promotion·OH、3SRHA*敏化作用Sensitization of ·OH, and 3SRHA*高浓度抑制High concentration inhibition光屏蔽Light-shield[50, 56][57-58][56]
此外,有研究提出DBC具有能带结构,可以通过光催化产生RIs。Guo等[36]研究了DBC带隙能量,DBC的导带能量高于O2/O2·-的还原电位,意味着O2可以转化为O2·-;DBC的价带能量低于OH-/·OH的氧化电位,表明·OH在可见光照射下很难产生。
4 溶解态黑碳的环境效应(Environmental effects of dissolved black carbon)
DBC是水体和土壤系统中活跃的化学组分之一,DBC在各环境介质中含量丰富,跨介质迁移能力强,对全球碳循环具有重要意义。此外,DBC富含羧基、羟基等活性基团,对疏水性有机污染物和重金属等有很强的亲和力,与这些污染物可以发生吸附或络合作用,影响其在环境中的迁移行为。DBC具有氧化还原能力和光化学活性,也可以通过光化学/物理过程生成光活性中间体,影响有机污染物在环境中转化行为。理解和全面认识DBC的环境效应,对准确预测全球碳循环及污染物的环境归趋具有重要意义。
4.1 溶解态黑碳对碳循环的影响(Effect of dissolved black carbon on carbon cycle)
土壤碳储量远高于大气碳储量,因此土壤碳循环过程中细微变化都将导致大气中CO2等温室气体浓度的变化[59]。黑碳在土壤固碳减排的作用方面已受到广泛关注。DBC作为黑碳水溶性组分,是黑碳循环的关键通量,不可避免地参与土壤固碳过程。DBC结构稳定性低于黑碳,因此降低了黑碳长期碳储存的潜力,影响土壤碳循环。环境中的化石燃料和生物质不完全燃烧生成烟尘,烟尘的2种主要成分是黑碳和有机碳。一部分烟尘进入大气,黑碳溶解于大气水相中释放DBC,导致DOC含量增加,最终随着大气对流、沉降等作用影响全球碳循环。另一部分则沉降在土壤、水体环境。同时大气沉降和地表径流等作用将大气与土壤中DBC引入水体,构成大气-土壤-河流海洋碳循环。海洋中DBC的循环是全球碳收支的重要组成部分。此外,DBC在全球河流有机碳通量的重要地位也暗示了在碳循环过程中的重要作用。现阶段迫切需要准确测量DBC稠芳香环结构的比例和运用模型模拟DBC的循环,以填补其在全球碳循环中知识的空白。动态全球植被模型是目前最先进的陆地生态系统碳循环模型,主要应用于全球及大陆尺度模拟[60]。模型-数据融合概念是降低陆地碳循环不确定性的有效途径,弥补了单独模拟的不足。
4.2 溶解态黑碳对污染物转化行为的影响(Effect of dissolved black carbon on pollutant transformation behavior)
4.2.1 溶解态黑碳对污染物的吸附作用(Adsorption of dissolved black carbon on pollutants)
土壤与河流底泥中的DBC对无机、有机污染物有多种吸附作用机制,包括比表面积和表面微孔结构的物理吸附作用、含氧官能团的化学吸附作用。DBC物理吸附环境中氧化铁等胶体离子,由于两者电荷相反,胶体离子表面电荷被中和,促进氧化铁胶体离子的聚集,增加其在环境中的稳定性[32]。DBC化学吸附涉及到疏水作用、氢键作用、配位螯合作用等多种机制,吸附非极性有机物以疏水作用为主。DBC对菲的吸附主要是脂肪碳链、芳环和醌基团或酯基团驱动的疏水相互作用、π-π电子供体-受体和化学分配作用[61]。DBC含有丰富的含氧基团和芳香族成分,氢键、疏水和π-π相互作用可以克服静电斥力,增强DBC吸附作用。Liu等[62-63]研究DBC对聚苯乙烯纳米塑料(polystyrene nanoplastics, PSs)聚集行为的影响,DBC可克服两者间的静电斥力,导致PSs吸附在DBC表面,降低PSs稳定性。此外,在DBC与金属配位体系中,DBC对有机物的吸附能力增强。DBC-Al(Ⅲ)体系促进DBC分子内和分子间的相互作用,形成类胶束结构,提高了对芘等疏水性有机污染物的分配系数[64]。
4.2.2 溶解态黑碳通过电子传递影响污染物的转化(Dissolved black carbon affects the transformation of pollutants through electron transfer)
DBC含有大量酚类、醌类等具有活泼的氧化还原能力组分,自身可作为电子传递载体或反应物参与污染物在环境中的氧化还原转化过程。DBC结构中的酚类和羧酸基团等组分可作为还原剂,直接还原环境中的Cr(Ⅵ)为Cr(Ⅲ);半醌自由基具有氧化活性,作为电子受体将As(Ⅲ)氧化为As(Ⅴ)[65]。DBC对Cr(Ⅵ)的还原和As(Ⅲ)的氧化过程降低了两者在环境中的毒性和流动性。DBC结构中的醌类和酚类基团还具有电子传递作用,提高Fe(Ⅲ)、二硫苏糖醇、二硝基类除草剂等污染物在环境中的还原速率[66]。DBC在细菌和含Fe(Ⅲ)矿物氧化还原过程中作为电子传递载体,接受细菌厌氧呼吸产生的电子,再将电子传递给矿物上的电子受体如Fe(Ⅲ),减少了重金属对细菌的毒害作用,并促进矿物中具有多种氧化态金属的生物循环[67-68]。
4.2.3 溶解态黑碳通过光致还原影响污染物的转化(Dissolved black carbon affects the transformation of pollutants through photoreduction)
光致还原途径是DBC在阳光下氧化还原污染物的另一重要途径。DBC结构中的有机成分与矿物组分协同光致生成O2·-,可还原Hg(Ⅱ)为Hg(0) [69],减少了植物对汞的吸收。在光照下,DBC促进了Ag+光还原为纳米银(nAg)途径,一方面是O2·-还原Ag+为nAg,另一方面是DBC对Ag+的吸附增强了配体金属电荷转移的过程[62]。
DBC氧化还原能力除受到自身结构的影响,也受到污染物氧化还原电位高低的影响。DBC还原作用主要针对氧化电位较高的污染物,DBC氧化作用主要针对氧化电位较低的污染物。Guo等[36]对DBC氧化还原四环素和亚甲基蓝结果差异进行了研究,发现四环素氧化电位低于亚甲基蓝,四环素失去电子所需能量更少,因此四环素更容易被DBC氧化。Graber等[70]的研究表明DBC可还原土壤中的Mn(Ⅱ)和Fe(Ⅲ),Mn的释放量高于Fe,这可能是因为Mn氧化物的还原电位大于Fe氧化物的还原电位。
4.2.4 溶解态黑碳对有机污染物光降解转化过程的影响(Effect of dissolved black carbon on photodegradation and transformation of organic pollutants)
DBC有效地介导酚类、医药品和个人护理品、内分泌干扰物等有机污染物的间接光降解过程。DBC中的生色组分可被光激发形成3DBC*、1O2、·OH和O2·-等。这些光活性中间体可以光敏化有机污染物,从而促进其光降解行为的发生。另一方面,DBC可以通过光屏蔽效应或者猝灭活性中间体等作用,抑制有机污染物的光降解过程。通过对反应中间产物的分析研究,探索DBC对污染物的光降解机制,这其中包含了RIs光敏化机制、氧化作用、光屏蔽作用和猝灭作用等机制。
(1)DBC对生物污染物——抗生素抗性基因(extracellular antibiotic resistance genes, eARGs)光降解转化过程的影响。除了紫外光诱导的DNA损伤外,RIs也可诱导DNA损伤。然而,在各种RIs (·OH、1O2、O2·-、H2O2)中,·OH和1O2是唯一能导致DNA损伤的物质。光照可以有效地光降解eARGs,DBC的存在加速了这一过程。DBC光敏化产生的·OH增强质粒链的断裂,而1O2加速了鸟嘌呤的氧化,促进了eARGs在水环境中的光降解,·OH和1O2的光降解贡献率与eARGs直接光解相当[71]。此外,高浓度的DBC一方面与eARGs竞争光子,抑制eARGs直接光解;另一方面高浓度DBC与·OH有较高的反应速率,并且高浓度DBC对1O2具有猝灭作用。因此,在高浓度下,DBC对RIs去除的贡献可能超过其对RIs产生的贡献。
(2)DBC对胺/酚类有机污染物光降解转化过程的影响。DBC促进胺/酚类有机污染物的光降解主要是由于3DBC*的电子转移作用。3DBC*与胺/酚类污染物之间的电子转移相互作用与胺的氮(N-电子)或酚的氧(O-电子)上的非键电子的可用性有关。对胺类化合物而言,光反应是由N-电子转移到3DBC*形成胺基阳离子,并进行快速的α-H转移引起的,有机碳阳离子自由基进一步导致C—N键断裂,生成脱烷基产物或被水攻击形成羟基化产物[29]。对酚类污染物而言,电子从酚环的O-电子转移到3DBC*,随后是发生质子的快速转移,导致苯氧基的形成[72-73]。此外,·OH可氧化酚类污染物的脱氧基、攻击芳香环和发生氧化作用,生成羟基化产物和氧化产物。
(3)DBC对微塑料光老化过程的影响。微塑料(microplastics, MPs)的光老化过程通常是C—C和C—H键在紫外光作用下断裂,与氧反应生成含氧基团(C—O),吸收周围环境中的氢,并形成氢过氧化物基团(—COOH),然后进一步分解成其他产物(如C![]() O、C—OH,O—C
O、C—OH,O—C![]() O)。因此,在紫外光的作用下,DBC可能会导致MPs的表面形成更多的含氧官能团,促进MPs的老化过程,也可能由于自由基清除作用和竞争吸收光子作用抑制MPs的老化。太阳光促进了DBC老化聚苯乙烯微塑料(polystyrene microplastic, PSMP)体系的电子转移,加速了O2·-和H2O2生成·OH的反应过程,增加·OH的强度并促进1O2的生成,促进PSMP表面含氧官能团的产生[74-75]。此外,DBC在黑暗条件下仍能产生少量的ROS,促进了PSMP的老化,这对于深层水体中MPs的老化研究具有重要参考意义。但总的来说,DBC对促进PSMP的老化作用在光照条件下更加明显。MPs化学结构的差异可能使DBC对其老化具有不同机制。研究表明,DBC对聚乙烯微塑料(polyethylene microplastics, PEMP)的老化具有抑制作用[76]。一方面使DBC对ROS的清除作用显著降低了PEMP在光照下形成·OH和1O2的能力;另一方面使DBC的光屏蔽作用减少了PEMP颗粒的破碎。
O)。因此,在紫外光的作用下,DBC可能会导致MPs的表面形成更多的含氧官能团,促进MPs的老化过程,也可能由于自由基清除作用和竞争吸收光子作用抑制MPs的老化。太阳光促进了DBC老化聚苯乙烯微塑料(polystyrene microplastic, PSMP)体系的电子转移,加速了O2·-和H2O2生成·OH的反应过程,增加·OH的强度并促进1O2的生成,促进PSMP表面含氧官能团的产生[74-75]。此外,DBC在黑暗条件下仍能产生少量的ROS,促进了PSMP的老化,这对于深层水体中MPs的老化研究具有重要参考意义。但总的来说,DBC对促进PSMP的老化作用在光照条件下更加明显。MPs化学结构的差异可能使DBC对其老化具有不同机制。研究表明,DBC对聚乙烯微塑料(polyethylene microplastics, PEMP)的老化具有抑制作用[76]。一方面使DBC对ROS的清除作用显著降低了PEMP在光照下形成·OH和1O2的能力;另一方面使DBC的光屏蔽作用减少了PEMP颗粒的破碎。
实际水体环境复杂,共存离子(如Cl-、Br-、HCO3-、NO3-和NO2-)会影响RIs浓度[77]。Cl-、Br-和HCO3-能清除·OH和3DBC*,而NO3-和NO2-可以被光激发产生·OH,说明在实际环境中DBC对污染物光化学转化的影响机制更加复杂。DBC影响污染物光转化途径如图2所示。

图2 溶解态黑碳影响环境污染物光化学转化行为
Fig. 2 Effects of dissolved black carbon on the phototransformation of contaminants in the environment
5 结论与展望(Conclusion and prospect)
综上所述,DBC是BC的溶解部分,广泛存在于各种环境介质中,介导多种物质的环境行为并参与全球碳循环。不同生物质衍生的DBC物理化学性质具有差异,但光化学活性和吸附能力优于研究充分的DOM。DBC广泛存在于各环境介质,影响污染物的环境行为,并参与全球碳循环。研究表明DBC对有机污染物降解与重金属还原具有积极意义,加强相关方面的研究可为难降解有机污染物的去除和解决碳收支平衡问题提供研究基础和技术支撑。
当前,对DBC的研究处于快速发展阶段,但研究深度和广度还有待加强,许多研究处于空白阶段。DBC介导污染物环境行为的相关机制缺乏统一的认知,DBC介导后的产物毒性变化、中间产物的性质、对微生物群落结构的方面也缺乏深入研究。总结相关研究进展,今后应加强以下几个方面的研究工作。
(1)DBC在微污染物光转化过程中的作用机理需要进一步阐明。目前对DBC介导有机污染物降解机制与还原重金属机理分析的认识尚浅,且在实际环境中存在多种机制共同作用。实际环境中的研究工作与机制研究存在差异。建议机制研究从理论方法(如量化)入手,实际环境中的研究涉及到多种环境因素的影响,单因素实验与中心组合实验结合分析对了解DBC在实际环境中的光转化具有重要意义。
(2)分析DBC降解不同类型有机污染物之间的机制差异研究。污染物种类繁多、结构各异、物理化学性质也千差万别。DBC作为光敏剂(猝灭剂)促进(抑制)污染物降解,作用机制的差异可能与污染物结构相关。目前研究多从DBC对一种物质的作用机理研究入手,缺乏DBC对不同污染物降解机制的系统比较分析。未来研究应重视DBC对不同类型有机物降解机制差异分析,以便更好了解DBC环境效应。
(3)加强DBC在全球碳循环中作用的研究。DBC具有一定的生物化学稳定性,在各类水体中浓度时空差异很大,占溶解有机碳比例也不相同。探清DBC的全球储量对全面理解DBC和碳循环具有重要意义。目前关于DBC的浓度监测数据还十分匮乏,难于准确估算全球DBC的储量。因此,获得更多的浓度监测数据对阐明DBC在全球碳循环中作用至关重要。
(4)DBC不可避免地参与许多污染物降解等环境行为,应该加强中间产物鉴定与最终产物毒性分析,采用模型预测DBC介导有机污染物光降解产物的生态风险。基于超高辨液质联用仪鉴定,获得DBC介导有机污染物光解产物的结构式,利用Chemical Draw软件获得降解产物的SMILES和CAS码。通过SMILES和CAS码,在ECOSAR和TEST软件(美国环境保护局)中计算有机污染物母体和DBC介导有机污染物光降解产物的毒性值。
[1] Xiao X, Chen B L, Chen Z M, et al. Insight into multiple and multilevel structures of biochars and their potential environmental applications: A critical review [J]. Environmental Science &Technology, 2018, 52(9): 5027-5047
[2] Alam M S, Gorman-Lewis D, Chen N, et al. Thermodynamic analysis of nickel(Ⅱ) and zinc(Ⅱ) adsorption to biochar [J]. Environmental Science &Technology, 2018, 52(11): 6246-6255
[3] Singh B P, Cowie A L, Smernik R J. Biochar carbon stability in a clayey soil as a function of feedstock and pyrolysis temperature [J]. Environmental Science &Technology, 2012, 46(21): 11770-11778
[4] Song Y, Wang F, Kengara F O, et al. Immobilization of chlorobenzenes in soil using wheat straw biochar [J]. Journal of Agricultural and Food Chemistry, 2013, 61(18): 4210-4217
[5] Jaffé R, Ding Y, Niggemann J, et al. Global charcoal mobilization from soils via dissolution and riverine transport to the oceans [J]. Science, 2013, 340(6130): 345-347
[6] Kim S, Kaplan L A, Benner R, et al. Hydrogen-deficient molecules in natural riverine water samples—Evidence for the existence of black carbon in DOM [J]. Marine Chemistry, 2004, 92(1-4): 225-234
[7] Hockaday W C, Grannas A M, Kim S, et al. Direct molecular evidence for the degradation and mobility of black carbon in soils from ultrahigh-resolution mass spectral analysis of dissolved organic matter from a fire-impacted forest soil [J]. Organic Geochemistry, 2006, 37(4): 501-510
[8] Dittmar T, de Rezende C E, Manecki M, et al. Continuous flux of dissolved black carbon from a vanished tropical forest biome [J]. Nature Geoscience, 2012, 5(9): 618-622
[9] Yamashita Y, Kojima D, Yoshida N, et al. Relationships between dissolved black carbon and dissolved organic matter in streams [J]. Chemosphere, 2021, 271: 129824
[10] Xu C L, Xue Y J, Qi Y Z, et al. Quantities and fluxes of dissolved and particulate black carbon in the Changjiang and Huanghe Rivers, China [J]. Estuaries and Coasts, 2016, 39(6): 1617-1625
[11] Ding Y, Yamashita Y, Jones J, et al. Dissolved black carbon in boreal forest and glacial rivers of central Alaska: Assessment of biomass burning versus anthropogenic sources [J]. Biogeochemistry, 2015, 123(1): 15-25
[12] Masiello C A, Druffel E R M. Black carbon in deep-sea sediments [J]. Science, 1998, 280(5371): 1911-1913
[13] 秦世广, 汤洁, 温玉璞. 黑碳气溶胶及其在气候变化研究中的意义[J]. 气象, 2001, 27(11): 3-7
Qin S G, Tang J, Wen Y P. Black carbon and its importance in climate change studies [J]. Meteorological Monthly, 2001, 27(11): 3-7 (in Chinese)
[14] Wagner S, Cawley K M, Rosario-Ortiz F L, et al. In-stream sources and links between particulate and dissolved black carbon following a wildfire [J]. Biogeochemistry, 2015, 124(1): 145-161
[15] Bao H Y, Niggemann J, Luo L, et al. Aerosols as a source of dissolved black carbon to the ocean [J]. Nature Communications, 2017, 8(1): 510
[16] Khan A L, Jaffé R, Ding Y, et al. Dissolved black carbon in Antarctic Lakes: Chemical signatures of past and present sources [J]. Geophysical Research Letters, 2016, 43(11): 5750-5757
[17] Fang Y, Chen Y J, Huang G P, et al. Particulate and dissolved black carbon in coastal China seas: Spatiotemporal variations, dynamics, and potential implications [J]. Environmental Science &Technology, 2021, 55(1): 788-796
[18] Drake T W, Wagner S, Stubbins A, et al. Du feu à l’Eau: Source and flux of dissolved black carbon from the Congo River [J]. Global Biogeochemical Cycles, 2020, 34(8): e2020GB006560
[19] 黄国培. 渤海水体中溶解态黑碳的时空分布与来源通量[D]. 北京: 中国科学院研究生院, 2016: 150-165
Huang G P. The spatial-temporal variations of dissolved black carbon in the Bohai Sea water, China and the river fluxes [D]. Beijing: Graduate School of Chinese Academy of Sciences, 2016: 150-165 (in Chinese)
[20] Xu F C, Wei C H, Zeng Q Q, et al. Aggregation behavior of dissolved black carbon: Implications for vertical mass flux and fractionation in aquatic systems [J]. Environmental Science &Technology, 2017, 51(23): 13723-13732
[21] Kaal J, Wagner S, Jaffé R. Molecular properties of ultrafiltered dissolved organic matter and dissolved black carbon in headwater streams as determined by pyrolysis-GC MS [J]. Journal of Analytical and Applied Pyrolysis, 2016, 118: 181-191
[22] Stubbins A, Spencer R G M, Mann P J, et al. Utilizing colored dissolved organic matter to derive dissolved black carbon export by Arcticrivers [J]. Frontiers in Earth Science, 2015, 3: 63
[23] Liu C H, Chu W Y, Li H, et al. Quantification and characterization of dissolved organic carbon from biochars [J]. Geoderma, 2019, 335: 161-169
[24] Qu X L, Fu H Y, Mao J D, et al. Chemical and structural properties of dissolved black carbon released from biochars [J]. Carbon, 2016, 96: 759-767
[25] Ji M Y, Zhou L, Zhang S C, et al. Effects of biochar on methane emission from paddy soil: Focusing on DOM and microbial communities [J]. The Science of the Total Environment, 2020, 743: 140725
[26] Lin Y, Munroe P, Joseph S, et al. Water extractable organic carbon in untreated and chemical treated biochars [J]. Chemosphere, 2012, 87(2): 151-157
[27] Lyu L L, Wen Z D, Jacinthe P A, et al. Absorption characteristics of CDOM in treated and non-treated urban lakes in Changchun, China [J]. Environmental Research, 2020, 182: 109084
[28] Weishaar J L, Aiken G R, Bergamaschi B A, et al. Evaluation of specific ultraviolet absorbance as an indicator of the chemical composition and reactivity of dissolved organic carbon [J]. Environmental Science &Technology, 2003, 37(20): 4702-4708
[29] Wan D, Wang J, Dionysiou D D, et al. Photogeneration of reactive species from biochar-derived dissolved black carbon for the degradation of amine and phenolic pollutants [J]. Environmental Science &Technology, 2021, 55(13): 8866-8876
[30] 杜紫嫣. 溶解态黑碳光化学活性预测模型研究[D]. 南京: 南京大学, 2018: 39-45
Du Z Y. A predictive model for photochemical activity of dissolved black carbon [D]. Nanjing: Nanjing University, 2018: 39-45 (in Chinese)
[31] Lian F, Xing B S. Black carbon (biochar) in water/soil environments: Molecular structure, sorption, stability, and potential risk [J]. Environmental Science &Technology, 2017, 51(23): 13517-13532
[32] Lian F, Yu W C, Wang Z Y, et al. New insights into black carbon nanoparticle-induced dispersibility of goethite colloids and configuration-dependent sorption for phenanthrene [J]. Environmental Science &Technology, 2019, 53(2): 661-670
[33] Fu H Y, Liu H T, Mao J D, et al. Photochemistry of dissolved black carbon released from biochar: Reactive oxygen species generation and phototransformation [J]. Environmental Science &Technology, 2016, 50(3): 1218-1226
[34] Norwood M J, Louchouarn P, Kuo L J, et al. Characterization and biodegradation of water-soluble biomarkers and organic carbon extracted from low temperature chars [J]. Organic Geochemistry, 2013, 56: 111-119
[35] Xu Y H, Ou Q, He Q, et al. Influence of dissolved black carbon on the aggregation and deposition of polystyrenenanoplastics: Comparison with dissolved humic acid [J]. Water Research, 2021, 196: 117054
[36] Guo Y, Guo Y, Hua S G, et al. Coupling band structure and oxidation-reduction potential to expound photodegradation performance difference of biochar-derived dissolved black carbon for organic pollutants under light irradiation [J]. The Science of the Total Environment, 2022, 820: 153300
[37] Hertkorn N, Frommberger M, Witt M, et al. Natural organic matter and the event horizon of mass spectrometry [J]. Geochimca et Cosmochimica Acta, 2008, 73(13): A526-A526
[38] Dittmar T, Koch B P. Thermogenic organic matter dissolved in the abyssal ocean [J]. Marine Chemistry, 2006, 102(3-4): 208-217
[39] Yang K J, Chen B L, Zhu X Y, et al. Aggregation, adsorption, and morphological transformation of graphene oxide in aqueous solutions containing different metal cations [J]. Environmental Science &Technology, 2016, 50(20): 11066-11075
[40] Wu L, Liu L, Gao B, et al. Aggregation kinetics of graphene oxides in aqueous solutions: Experiments, mechanisms, and modeling [J]. Langmuir: The ACS Journal of Surfaces and Colloids, 2013, 29(49): 15174-15181
[41] Qian L B, Zhang W Y, Yan J C, et al. Effective removal of heavy metal by biochar colloids under different pyrolysis temperatures [J]. Bioresource Technology, 2016, 206: 217-224
[42] Jia F, Gan J. Comparing black carbon types in sequestering polybrominated diphenyl ethers (PBDEs) in sediments [J]. Environmental Pollution, 2014, 184: 131-137
[43] Xu Y H, Ou Q, Liu C H, et al. Aggregation and deposition behaviors of dissolved black carbon with coexisting heavy metals in aquatic solution [J]. Environmental Science: Nano, 2020, 7(9): 2773-2784
[44] Fu H Y, Wei C H, Qu X L, et al. Strong binding of a polar hydrophobic organic contaminants by dissolved black carbon released from biochar: A mechanism of pseudomicelle partition and environmental implications [J]. Environmental Pollution, 2018, 232: 402-410
[45] Tang J F, Li X H, Luo Y, et al. Spectroscopic characterization of dissolved organic matter derived from differentbiochars and their polycylic aromatic hydrocarbons (PAHs) binding affinity [J]. Chemosphere, 2016, 152: 399-406
[46] Pan B, Xing B S, Liu W X, et al. Investigating interactions of phenanthrene with dissolved organic matter: Limitations of Stern-Volmer plot [J]. Chemosphere, 2007, 69(10): 1555-1562
[47] Luo L, Chen Z E, Lv J T, et al. Molecular understanding of dissolved black carbon sorption in soil-water environment [J]. Water Research, 2019, 154: 210-216
[48] Sun Y Q, Xiong X N, He M J, et al. Roles of biochar-derived dissolved organic matter in soil amendment and environmental remediation: A critical review [J]. Chemical Engineering Journal, 2021, 424: 130387
[49] Zheng X J, Liu Y F, Fu H Y, et al. Comparing electron donating/accepting capacities (EDC/EAC) between crop residue-derived dissolved black carbon and standard humic substances [J]. The Science of the Total Environment, 2019, 673: 29-35
[50] Zhou Z C, Chen B N, Qu X L, et al. Dissolved black carbon as an efficient sensitizer in the photochemical transformation of 17β-estradiol in aqueous solution [J]. Environmental Science &Technology, 2018, 52(18): 10391-10399
[51] Kang S, Xing B S. Adsorption of dicarboxylic acids by clay minerals as examined by in situ ATR-FTIR and ex situ DRIFT [J]. Langmuir: The ACS Journal of Surfaces and Colloids, 2007, 23(13): 7024-7031
[52] Stubbins A, Niggemann J, Dittmar T. Photo-lability of deep ocean dissolved black carbon [J]. Biogeosciences, 2012, 9(5): 1661-1670
[53] Wan D, Sharma V K, Liu L, et al. Mechanistic insight into the effect of metal ions on photogeneration of reactive species from dissolved organic matter [J]. Environmental Science &Technology, 2019, 53(10): 5778-5786
[54] Tian Y J, Feng L, Wang C, et al. Dissolved black carbon enhanced the aquatic photo-transformation of chlortetracycline via triplet excited-state species: The role of chemical composition [J]. Environmental Research, 2019, 179(Pt B): 108855
[55] Li M, Bao F X, Zhang Y, et al. Photochemical aging of soot in the aqueous phase: Release of dissolved black carbon and the formation of 1O2 [J]. Environmental Science &Technology, 2019, 53(21): 12311-12319
[56] 梁辰. 溶解性有机质对不同解离形态诺氟沙星光降解的影响[D]. 大连: 大连理工大学, 2014: 9-10
Liang C. Effect of dissolved organic matters on photolysis of norfloxacin with different dissociation species [D]. Dalian: Dalian University of Technology, 2014: 9-10 (in Chinese)
[57] Janssen E M L, Erickson P R, McNeill K. Dual roles of dissolved organic matter as sensitizer and quencher in the photooxidation of tryptophan [J]. Environmental Science &Technology, 2014, 48(9): 4916-4924
[58] 赵健辰. 溶解性有机质光致生成活性物种机理及量子产率的定量构效关系模型研究[D]. 长春: 东北师范大学, 2020: 4-5
Zhao J C. Photochemical generation mechanisms and quantum yield quantitative structure-activity relationship models of reactive species from dissolved organic matter [D]. Changchun: Northeast Normal University, 2020: 4-5 (in Chinese)
[59] 李怡安, 胡华英, 周垂帆. 浅析生物炭对土壤碳循环的影响[J]. 内蒙古林业调查设计, 2019, 42(5): 102-104
Li Y A, Hu H Y, Zhou C F. Analysis of the effects of biochar on soil carbon cycle [J]. Inner Mongolia Forestry Investigation and Design, 2019, 42(5): 102-104 (in Chinese)
[60] Sakaguchi K, Zeng X, Leung L R, et al. Influence of dynamic vegetation on carbon-nitrogen cycle feedback in the Community Land Model (CLM4) [J]. Environmental Research Letters, 2016, 11(12): 124029
[61] Chen Q, Ma Y J, Dong J H, et al. The chemical structure characteristics of dissolved black carbon and their binding with phenanthrene [J]. Chemosphere, 2022, 291(Pt 1): 132747
[62] Liu H T, Ge Q, Xu F C, et al. Dissolved black carbon induces fast photo-reduction of silver ions under simulated sunlight [J]. Science of the Total Environment, 2021, 775: 145897
[63] Liu Y J, Huang Z Q, Zhou J N, et al. Influence of environmental and biological macromolecules on aggregation kinetics of nanoplastics in aquatic systems [J]. Water Research, 2020, 186: 116316
[64] Pan B, Ghosh S, Xing B S. Dissolved organic matter conformation and its interaction with pyrene as affected by water chemistry and concentration [J]. Environmental Science &Technology, 2008, 42(5): 1594-1599
[65] Dong X L, Ma L Q, Gress J, et al. Enhanced Cr(Ⅵ) reduction and As(Ⅲ) oxidation in ice phase: Important role of dissolved organic matter from biochar [J]. Journal of Hazardous Materials, 2014, 267: 62-70
[66] Oh S Y, Son J G, Chiu P C. Biochar-mediated reductive transformation of nitro herbicides and explosives [J]. Environmental Toxicology and Chemistry, 2013, 32(3): 501-508
[67] Kolton M, Meller Harel Y, Pasternak Z, et al. Impact of biochar application to soil on the root-associated bacterial community structure of fully developed greenhouse pepper plants [J]. Applied and Environmental Microbiology, 2011, 77(14): 4924-4930
[68] Graber E R, Harel Y M, Kolton M, et al. Biochar impact on development and productivity of pepper and tomato grown in fertigated soilless media [J]. Plant and Soil, 2010, 337(1): 481-496
[69] Li L L, Wang X J, Fu H Y, et al. Dissolved black carbon facilitates photoreduction of Hg(Ⅱ) to Hg(0) and reduces mercury uptake by lettuce (Lactuca sativa L.) [J]. Environmental Science &Technology, 2020, 54(18): 11137-11145
[70] Graber E R, Tsechansky L, Lew B, et al. Reducing capacity of water extracts of biochars and their solubilization of soil Mn and Fe [J]. European Journal of Soil Science, 2014, 65(1): 162-172
[71] Zhang X, Li J, Fan W Y, et al. Enhanced photodegradation of extracellular antibiotic resistance genes by dissolved organic matter photosensitization [J]. Environmental Science &Technology, 2019, 53(18): 10732-10740
[72] Canonica S, Hellrung B, Wirz J. Oxidation of phenols by triplet aromatic ketones in aqueous solution [J]. The Journal of Physical Chemistry A, 2000, 104(6): 1226-1232
[73] Canonica S, Jans U, Stemmler K, et al. Transformation kinetics of phenols in water: Photosensitization by dissolved natural organic material and aromatic ketones [J]. Environmental Science &Technology, 1995, 29(7): 1822-1831
[74] Qiu X R, Ma S R, Zhang J X, et al. Dissolved organic matter promotes the aging process of polystyrene microplastics under dark and ultraviolet light conditions: The crucial role of reactive oxygen species [J]. Environmental Science &Technology, 2022, 56(14): 10149-10160
[75] Zhu K C, Jia H Z, Sun Y J, et al. Long-termphototransformation of microplastics under simulated sunlight irradiation in aquatic environments: Roles of reactive oxygen species [J]. Water Research, 2020, 173: 115564
[76] Wu X W, Liu P, Gong Z M, et al. Humic acid and fulvic acid hinder long-term weathering of microplastics in lake water [J]. Environmental Science &Technology, 2021, 55(23): 15810-15820
[77] Parker K M, Mitch W A. Halogen radicals contribute to photooxidation in coastal and estuarine waters [J]. Proceedings of the National Academy of Sciences of the United States of America, 2016, 113(21): 5868-5873